



3.3.5. Нейтрализация сульфомассы.
Реакционная масса после сульфирования содержит целевой продукт - сульфокислоту и непрореагировавший сульфирующий агент. С целью отделения целевой сульфокислоты реакционная масса подвергается одному из видов обработки: нейтрализации, разбавлению водой или высаливанию сульфокислот.
Нейтрализующими агентами служат: кальцинированная сода (Na2CO3), сульфит натрия (Na2SO3), мел, известь и водные растворы аммиака. Для высаливания используют сульфат натрия (Na2SO4) и Na Cl. Технология нейтрализации сульфомассы. например, сульфитом натрия заключается в следующем. К сульфомассе постепенно приливают нагретый до 100 °С раствор сульфита натрия. Нейтрализация массы сопровождается выделением сернистого газа (SO2), который направляется в систему улавливания. При нейтрализации сульфомассу выдерживают некоторое время при температуре 100 °С, после загрузки сульфита натрия для полного выделения сернистого газа. Для поддержания необходимой температуры аппарат снабжается змеевиком или рубашкой.
Также для нейтрализации сульфомасс используют суспензию мела в воде. Выделяемое при нейтрализации тепло компенсирует потери тепла с удаляющимся углекислым газом, поэтому такие нейтрализаторы не имеют теплообменных устройств.
Иногда сульфокислоту требуется из реакционной массы в виде натриевой или калиевой соли, так называемым методом высаливания. Для этого к сульфомассе приливают раствор хлористого натрия или калия. Часто высаливание проводят по следующей технологии: сульфомассу разбавляют водой, а затем добавляют соли (хлориды и сульфаты натрия или калия). Реакция солеобразования протекает по следующему типу :
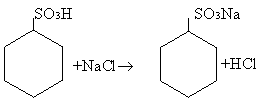
Соль расходуется больше, чем это соответствует стехиометрии, приведенному выше уравнению. Это объясняется тем, что часть соли вступает в химическое взаимодействие с сульфокислотой, а другая часть растворяется в воде, понижая растворимость солей образованных в результате реакции. Эти соли выпадают в осадок, а затем фильтрованием отделяются от жидкой фазы.
Сульфокислота может выделяться из сульфомассы также и разбавлением водой. Этот способ основан на свойстве некоторых сульфокислот растворяться в концентрированном сульфоагенте и выпадать в осадок при слабой концентрации его. Поэтому в сульфомассу добавляют воду, снижая концентрацию серной кислоты (сульфоагента).
Выделение сульфокислот водой проводят в тех же условиях и в той же аппаратуре, что и разбавление кислот (см. выше).
|
|
|
|