



4. НИТРОВАНИЕ
4.1. Общие понятия о нитровании.
Нитрование - процесс замещения атома водорода в молекуле органического вещества нитрогруппой NO3. В качестве органических веществ используют при этом незамещенные и замещенные ароматические углеводороды: бензол, толуол, нафталин, хлорбензол, фенол, сульфокислоты нафталина. Нитрующими агентами являются: азотная кислота, а также нитрующие смеси, содержащие азотную кислоту, серную кислоту и воду.
Реакция нитрования вещества нитрующей смесью описывается следующим уравнением:
RHx+x× HNO3+y× H2SO4+z× H2O = R(NO2)+y× H2SO4+(z+x)H2O
M1 63× x 98× y 18× z M2 98× y 18× (z+x)Азотная кислота при нитровании расходуется в соответствии со стехиометрией выше приведенного уравнения. Серная кислота не участвует в химическом взаимодействии с углеводородом, но ее присутствие в определенном количестве необходимо при нитровании большинства ароматических соединений. Процесс нитрования протекает гладко при строго определенной концентрации
H2SO4, т.е. при строго определенном отношении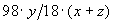 . Это отношение называется числом водоотнятия, которое и определяет концентрацию серной кислоты.
. Это отношение называется числом водоотнятия, которое и определяет концентрацию серной кислоты.
Следует отметить, что образующиеся нитропродукты, как правило, нерастворимы в отработанной серной кислоте и легко отделяются от нее путем отстаивания. Разбавленная серная кислота после отстаивания концентрируется и возвращается в цикл.
На основании вышеизложенного, эскизную технологическую схему нитрования углеводород можно представить в следующем виде:
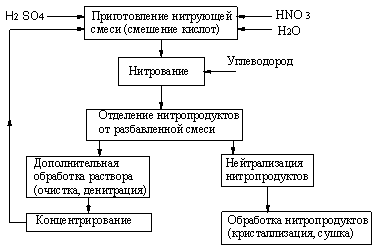
Рассмотрим некоторые стадии и аппаратурное оформление этой технологической схемы.
Смотрите дополнительную информацию|
|
|
|