



Задание: рассчитать материальный баланс стадии восстановления
2,4,5-трихлорнитробензола. Производительность по 2,4,5-трихлоранилину 10 т/год
|
Загружено: |
м.д.(W) |
g ,т/м3 |
|
|
1. |
Технич. 2,4,5-трихлорнитробенз. |
1.576 |
|
|
а) 2,4,5-трихлорнитробензол |
0,97 |
||
|
б) примеси |
0,03 |
||
|
2. |
Вода |
1 |
1 |
|
3. |
Чугунная стружка. |
1 |
7.0 |
|
4.* |
Соляная кислота от общей массы |
0,089 |
1.114 |
|
а) хлороводород |
27,5 |
||
|
б) вода |
72,5 |
*-
пункт 4 не учитываются уравнением реакции.Получены целевые продукты :
|
№ |
Целевой продукт |
кол-во |
|
1. |
2,4,5-трихлоранилин |
10 т. |
|
2. |
окись-закись железа |
? |
Получены побочные продукты *:
|
№ |
Побочный продукт |
м.д.(W) |
|
1. |
2,4,5-трихлорнитробензол |
0,0001 |
|
2. |
осмол |
0,03 |
|
3. |
примеси |
0,0072 |
|
4. |
хлористое железо |
0,0172 |
Решение:
Восстановление 2,4,5-трихлорнитробензола
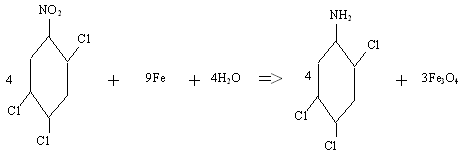
Уравнение реакции в упрощённом виде
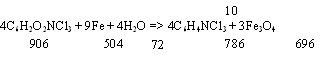
I. 2,4,6-трихлоранилин.
1. Найдем молярную массу образовавшегося 2,4,6-трихлоранилина.
M(2,4,6-трихлоранилина)=v*(Мr(С)*6 +Мr(H)*4 +Мr(N)*1+ Мr(Сl)*3)
M(2,4,6-трихлоранилина)=4*(12*6+1*4+14*1+35,5*3)=786
II. 2,4,5-трихлорнитробензол.
1.Найдем молярную массу 2,4,5-трихлорнитробензола.
M(2,4,5-трихлорнитробензола.)=v*(Мr(С)*6+ Мr(H)*2+ Мr(O)*2+ Мr(N)*1+ Мr(Сl)*3)
M(2,4,5-трихлорнитробензола)=4*(12*6+1*2+16*2+14*1+35,5*3)=906
2. Найдем массу 2,4,5-трихлорнитробензола, вступившей в реакцию.
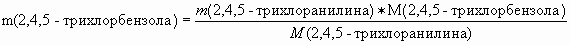

3. Найдем массу технического 2,4,5-трихлорнитробензола (первый пункт таблицы).
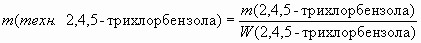
![]()
4. Найдем массу примеси в ![]()
m(примесей)=m(![]() )- m(
)- m(![]() )
)
m(примесей)=11,883-11,527=0,356
III. Железо.
1.Найдем молярную массу железа.
M(железа)=v*(Мr(Fe)*1)
M(железа)=9*(56*1)=504
2. Найдем массу железа, вступившего в реакцию.
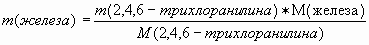
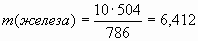
IV. Вода.
1.Найдем молярную массу воды.
M(воды)=v*(Мr(Н)*2+ Мr(О)*1)
M(воды)=4*(1*2+16*1)=72
2. Найдем массу воды, вступившей в реакцию.
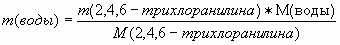
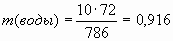
V. Окись-закись железа.
1.Найдем молярную массу окиси-закиси железа.
M(окиси-закиси железа)=v*(Мr(Fe)*3+ Мr(O)*4)
M(окиси-закиси железа)=3*(56*3+16*4)=696
2. Найдем массу образовавшегося окиси-закиси железа.
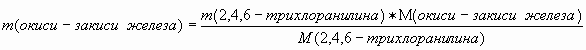
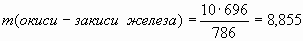
VI. Содержание веществ после реакции.
Масса всех веществ после реакции равна массе веществ до реакции.
М(всех веществ)= M(прореаг. веществ)+ m(соляной кислоты)
m(соляной кислоты)= М(прореаг. веществ)*W(соляной кислоты)
М(прореаг. веществ)= m(2,4,6-трихлоранилина)+ ![]() + m(примесей)=10+8,855+0,356=19,211
+ m(примесей)=10+8,855+0,356=19,211
m(соляной кислоты)=19.211**0,089=1.7
М(всех веществ)=19,211+1,7=20,911
1.2,4,6-трихлоранилин ![]()
![]()
2.Окиси-закиси железа 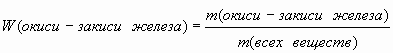
![]()
VII. Соляная кислота.
1. Найдем массу хлороводорода в соляной кислоте.
![]()
![]()
![]()
VIII. Побочные продукты.
1. 2,4,6-трихлорнитробензол
![]()
![]() 20,911*0,0001= 0,00209 [т].
20,911*0,0001= 0,00209 [т].
2.Осмол: ![]()
![]() =20,911*0,03= 0,627 [т].
=20,911*0,03= 0,627 [т].
3.Примеси: ![]()
![]() 20,911*0,0072= 0,15 [т].
20,911*0,0072= 0,15 [т].
4. Хлористое железо: ![]()
![]() 20,911*0,0172=0,36 [т].
20,911*0,0172=0,36 [т].
|
Номер пункта,части |
II |
|
III |
|
IV |
|
I,VII |
|
VII |
|
|
Масса всех примесей и непрореагирововшего в-ва |
0,356 |
|
||||||||
|
4) Масса примесей илимасса непрореагировавшего в-ва |
0,356 |
0,000 |
0,000 |
|||||||
|
m(примесей) |
||||||||||
|
Масса загруженных веществ Входящих в уравнение реакции |
19,211 |
19,211 |
||||||||
|
3)Масса загруженного в-ва |
11,883 |
6,412 |
0,916 |
|
|
|||||
|
Содержание в исходном растворе |
0,97 |
1,000 |
1,000 |
0,521 |
0,461 |
|||||
|
2)Масса веществ m(веществ) |
11,527 |
6,412 |
0,916 |
10,000 |
8,855 |
|||||
|
Уравнение |
4C6H2O2NCL3 + 9Fe + 4H2O => 4C6H4NCL3 + 3Fe3O4 |
|||||||||
|
Название |
2,4,5-трихлорбензол |
Железо |
Вода |
2,4,6-трихлоранилин |
Окись-закись железа |
|||||
|
Молекулярная масса(Mr) |
226,5 |
56,0 |
18,0 |
196,5 |
232,0 |
|||||
|
1)Молярная масса(М) |
906 |
504 |
72 |
786 |
696 |
|||||
IX. Результаты расчетов сведем в таблицу.
|
Загружено: [т] |
Получено: [т] |
||||
|
1. |
Технич. 2,4,5-трихлорнитробенз. |
11,883 |
1. |
2,4,6-трихлоранилин |
10 |
|
а) 2,4,5-трихлорнитробензол |
11,527 |
2. |
Окись-закись железа |
8,855 |
|
|
б) примеси |
0,356 |
3. |
Примеси |
1,139 |
|
|
2. |
Вода |
0,916 |
а) 2,4,5-трихлорнитробензол |
0,00209 |
|
|
3. |
Чугунная стружка. |
6,412 |
б) осмол |
0,627 |
|
|
4. |
Соляная кислота от общей массы |
1,7 |
в) примеси |
0,15 |
|
|
а) хлороводород |
0,47 |
г) хлористое железо |
0,36 |
||
|
б) вода |
1,23 |
||||
|
ИТОГО: |
20,9 |
ИТОГО: |
20,0 |
||
X. Выбор аппарата.
Примем рабочих дней в году t =290 суток.
![]() , где
, где
![]()
![]() -запас производительности
-запас производительности
![]()
![]() - время пребывания в реакционном аппарате (из регламента)
- время пребывания в реакционном аппарате (из регламента)
![]()
![]() =184+10+20+60+20+90+15+360+360+90+180+80+20+20+40+40=23ч 40 мин.
=184+10+20+60+20+90+15+360+360+90+180+80+20+20+40+40=23ч 40 мин.
![]() - степень заполнения 0,75
- степень заполнения 0,75
n- число аппаратов
![]() -годовой объём аппарата
-годовой объём аппарата
![]()
![]() = 10,89 м3
= 10,89 м3
![]()
![]()
Примем аппарат с объёмом 0,063 м3
D=800 мм
L=1325 мм
l=1100 мм
Площадь внутренней поверхности= 4,03м3
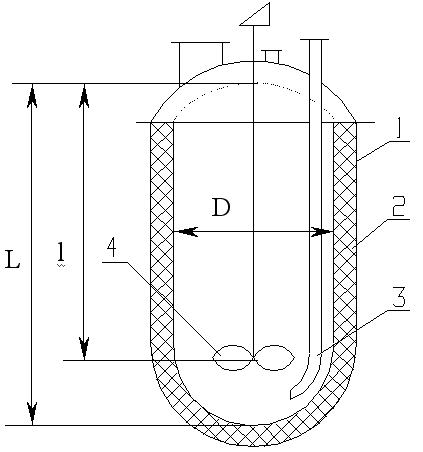
Редуктор для восстановления водо-растворимых соединений: 1 - стальной корпус; 2 -футеровка; 3 - труба передавливания; 4 - мешалка.
|
|
|
|